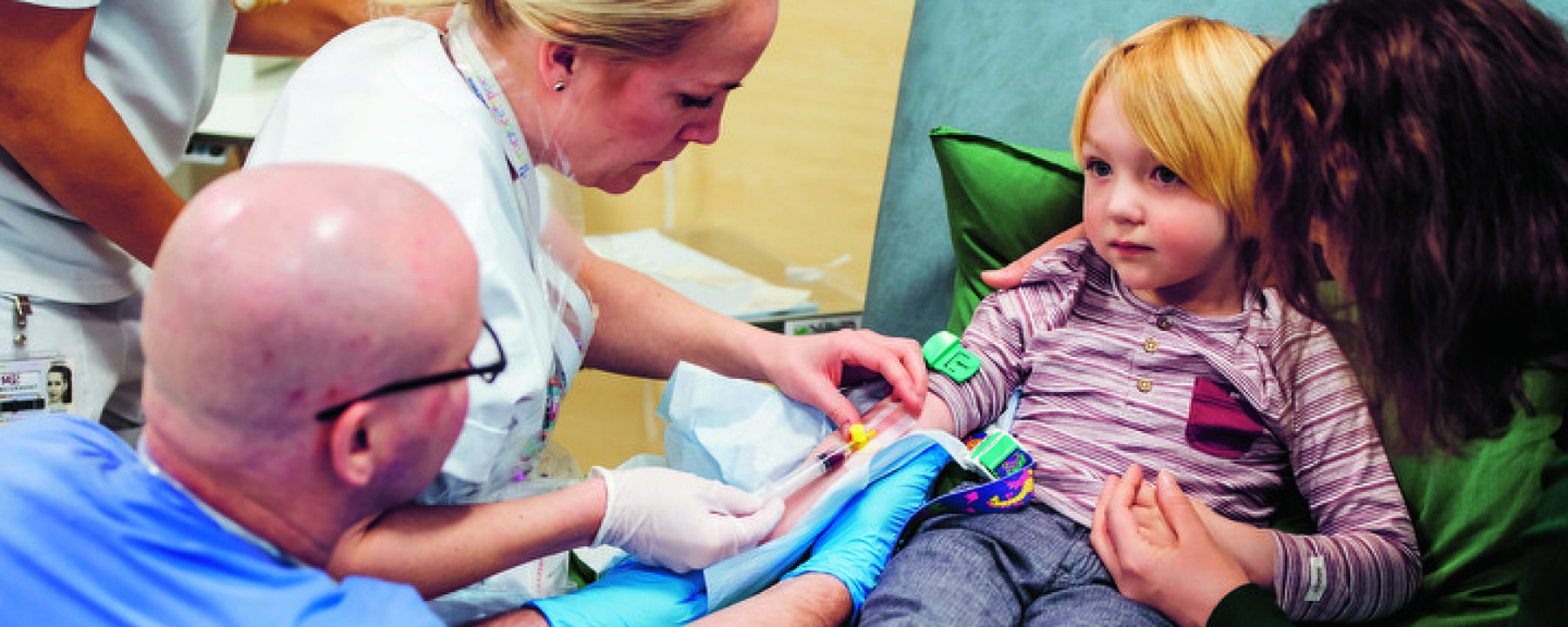
ALK-hämmarna: livräddare med färre biverkningar
Från dödligt sjuk av biverkningar till friskförklarad. När det första barnet behandlades med ALK-hämmare på Astrid Lindgrens barnsjukhus var det som ett mirakel. Nu tror barnonkolog Per Kogner på en framtid där nästan alla barn räddas, och där biverkningarna är mycket lindrigare.
Under 2014 kom en drygt ettårig pojke in till Astrid Lindgrens barnsjukhus. Undersökningar visade att han hade aggressiv, spridd cancer av typen neuroblastom. Det är en ovanlig cancerform som kan uppstå i sympatiska nervsystemet hos små barn. Pojken hade den allvarligaste formen, som bara varannan drabbad överlever.
Genast inleddes en tuff cytostatikabehandling. Föräldrarna fick höra att han skulle må dåligt av medicinen, men snart återhämta sig efter varje behandlingsomgång. Det gjorde han inte. Vilfred blev bara sämre och sämre. Efter den tredje cytostatikadosen på en månad blev han dödligt sjuk, och i nästan ett halvår flyttades han fram och tillbaka mellan barncanceravdelningen och intensivvårdsavdelningen. I flera månader behövde han blodtransfusioner varje dag.
– Om du frågar personalen på avdelningen kommer de att säga att de aldrig har haft en så svårt sjuk patient. Det är ju sånt man kan säga ibland. Men i det här fallet är det verkligen sant, säger Per Kogner.
Han är professor vid Karolinska Institutet och överläkare barnonkologi. Det var tydligt för honom och kollegorna att det var något annorlunda med Vilfred. Man beslöt att göra en helgenomsekvensering, en kartläggning av arvsmassan i cancercellerna. I dag görs det för alla barn som får en cancerdiagnos, men 2014 gjordes det bara i vissa fall. I det här fallet hade läkarna börjat misstänka att Vilfreds cancer berodde på genetiska mutationer som kunde behandlas med ett helt annat läkemedel.
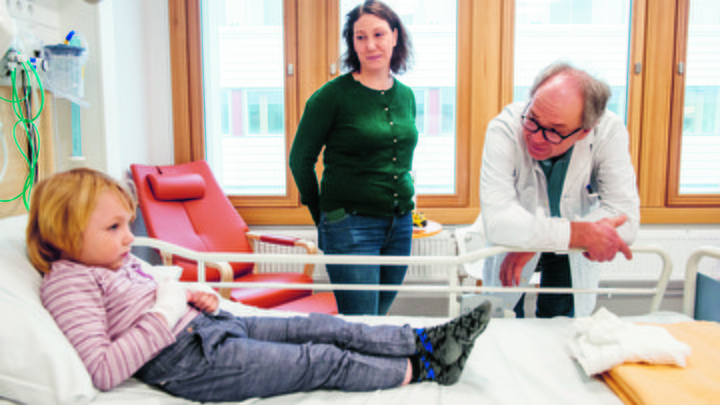
En avgörande mutation
Neuroblastom beror alltid på förändringar i vissa cellers DNA som förvandlar dem till cancerceller, men det är inte samma förändringar hos alla patienter. När svaret kom från Vilfreds analys var beskedet både allvarligt och hoppingivande. Vilfred hade ett genetiskt tillstånd kallat Fanconis anemi, som gör att kroppen är sämre än normalt på att reparera skador på arvsmassan. Det betyder att risken för cancer ökar, men också att patienten blir väldigt känslig för cytostatikabehandling eftersom den ofta verkar just genom att angripa DNA i snabbväxande celler. Vilfred tålde helt enkelt inte sin medicin.
Analysen visade också något annat: en mutation i genen för ett protein kallat ALK. Det betydde att det fanns en helt annan typ av behandling, ett nytt precisionsläkemedel, som kanske kunde vara räddningen.
Förkortningen ALK står för anaplastiskt lymfomkinas. Det är en molekyl som går genom ytan i nervceller och fungerar som receptor för en molekyl utanför. När den binder in till ALK startas en process inuti cellen. Processen är viktig vid utvecklingen av nervsystemet, och normalt är ALK bara aktiv under en del av fosterutvecklingen. Men vid mitten av 1990-talet upptäcktes att molekylen också spelade en viktig roll i flera cancerformer, bland annat lymfom (därav namnet). Mutationer i genen som kodar för ALK kan leda till att receptorn är ständigt aktiv, vilket kraftigt stimulerar tillväxten och får cellen att förvandlas till en tumörcell.
– Det är som en gaspedal för cellen. En ALK-mutation kan till exempel få receptorn att ändra form på cellens utsida så att den kopplar ihop sig med en annan molekyl som felaktigt aktiverar den. En annan mutation kan göra så att ALK aktiveras utan att binda till något alls. Beroende på typ av mutation kan man säga att gaspedalen låser sig olika hårt, säger Per Kogner.
Läkemedel mot lungcancer blev räddningen
2008 upptäckte två forskargrupper i världen, bland annat en i Sverige där Per Kogner och genetikprofessorn Tommy Martinsson ingick, att en till cancertyp kunde uppstå vid ALK-mutationer: neuroblastom.
En cancerform som beror på onormal aktivitet hos en receptor bör kunna behandlas med läkemedel som blockerar receptorn. Men att driva utvecklingen av läkemedel särskilt riktade mot barncancer är utmanande eftersom patienterna är så få. I Sverige får 350 barn per år cancer, omkring 6 procent av dem får neuroblastom, och knappt 10 procent av neuroblastompatienterna har en ALK-mutation.
När kopplingen mellan ALK och neuroblastom upptäcktes 2008 var medicinutvecklingen dock redan i full gång för en helt annan och mycket större patientgrupp. 2011 kom den första ALK-hämmaren för patienter med icke-småcellig lungcancer. Läkemedlet blockerar ALK-receptorns tillgång till ATP, en molekyl som förser cellens processer med energi. Utan energin upphör ALK-aktiviteten och cellerna omformas till vanliga, friska celler.
2014, när Vilfred låg inlagd på Astrid Lindgrens barnsjukhus, fanns redan en andra generation ALK-hämmare på marknaden. Men de hade ytterst sällan använts på barn, och inte på några barn alls i Sverige. Per Kogner startade den komplicerade process som krävdes för att få tillgång till behandlingen, och rätt att ge den till en pojke som dessutom var så sjuk att han nätt och jämnt mötte läkemedelsföretagets kriterier för behandling.
Till sist gick det. Då hade alla tillstånd sökts, en mängd tester gjorts, och i Göteborg hade neuroblastomforskaren Bengt Hallberg i sitt laboratorium skapat genmodifierade celler med samma mutation som Vilfred hade, för att kontrollera att läkemedlet verkade blockera just den sortens aktivering.
När Vilfred började få regelbundna injektioner med ALK-hämmare minskade storleken på hans tumörer gradvis, tills de blev möjliga att operera. Cancercellerna i nervsystemet mognade ut till friska celler. Biverkningarna var minimala, lite magproblem bara.
”Han mår bra nu”
Per Kogner minns ett återbesök då han på grund av fullbokade rum på mottagningen istället behövde ta emot Vilfred och hans föräldrar i ett litet rum på vårdavdelningen där pojken tidigare hade legat. Medan samtalet pågick därinne spred sig ryktet bland personalen: Vilfred är här i dag!
– När vi kom ut ur rummet stod hela personalen på rad bara för att få titta på honom. Då visste de: ”Vilfred har fått ny medicin. Och han mår bra nu.” Jag blir rörd när jag minns känslan.
En tid senare beslöt Per Kogner och hans kollegor att avsluta behandlingen. På avdelningen är det tradition när en behandling avslutas och ett barn ska hem att ringa i en klocka för att fira. Vilfred ville inte ringa själv, men satt i mammas famn och såg på när pappa gjorde det. Per Kogner stod bredvid.
– ”Tänk att vi kom till den här punkten”, tänkte jag då.
När den här artikeln skrivs har det gått fyra år, och Vilfred är fortfarande fri från cancer.

Varje fall ger ny kunskap
Dagens precisionsmedicinska behandlingar bygger på många års grundforskning kring cellers signalsystem och människans genetik. ALK-hämmare har hittills getts till omkring femton barn i Sverige, så få att varje behandling fortfarande ger nya kunskaper och leder till vetenskapliga artiklar. Per Kogner och hans kollegor har nyligen levererat en om de fem första barnen i Sverige som fått ALK-hämmare som monoterapi. Det betyder att hämmaren gavs som enda behandling, inte i kombination med exempelvis strålning eller cytostatika. Alla de fem fick hämmare antingen för att de återfallit i sin sjukdom, eller för att vanlig cytostatikabehandling inte hjälpte. Alla svarade på den nya behandlingen.
– Som försiktig forskare skulle jag säga att vi har lovande resultat. Som blödig läkare skulle jag kalla dem fantastiska. I min värld är det här det allra bästa exemplet på precisionsmedicin, säger Per Kogner.
Nästa steg är att ge ALK-hämmare som första linjens behandling, alltså som allra första alternativ. Patienter från svenska sjukhus kommer att ingå i en europeisk studie där alla barn med nydiagnostiserat neuroblastom får genomgå en helgenomsekvensering – något som redan görs i Sverige. De som visar sig bära en ALK-mutation ska sedan få ALK-hämmare utan föregående cytostatika.
Fler räddade liv, mindre biverkningar
På sikt räknar Per Kogner med att precisionsmedicin ska rädda i stort sett alla cancersjuka barn. Över 99 procent, har han vågat säga. Han ser också en stor potential för lindrigare behandlingar i stället för de av dagens terapier som är effektiva, men plågsamma.
– De 85 procent som redan botas ska ju ha inga eller rimliga biverkningar. En del har verkligen orimliga biverkningar, eftersom dagens behandlingar slår mot alla celler som delar sig. Ju mer spetsig den moderna behandlingen blir desto bättre, för då slipper man det. Barn ska inte behöva tappa håret eller förlora tarmslemhinnan.
Men det blir dyrt, konstaterar Per Kogner. Sjukvården kommer att kosta mer i framtiden. Det tycker han det är värt, med tanke på hur många levnadsår man räddar när ett litet barn klarar sig igenom sin cancersjukdom.
– Eller så kan man låta bli att räkna och bara känna efter, säger Per Kogner och ler lite.
För att nå fram behövs ännu mer grundforskning, ännu fler läkemedel, och fler läkemedelsstudier där barn ingår.
– De kommande stegen måste vi nästan ta ett barn i taget. Det är komplicerade lås, men vi smider nya nycklar hela tiden. Jag är övertygad om att det kommer att fungera.