Nytt analysverktyg kan ge bättre och mer riktad behandling av ALL
ALL, akut lymfatisk leukemi, är den vanligaste barncancern och innebär att vissa typer av immunceller börjar växa på ett okontrollerat sätt i benmärgen och tränger ut den friska blodbildningen. Nu har forskare på Karolinska Institutet tagit fram ett analysverktyg som kan bidra till bättre behandling för de barn som inte svarar på standardbehandlingen.
De flesta ALL-patienter kan behandlas med cytostatika (kemoterapi) och stamcellstransplantation men cirka 15 procent svarar dåligt på dessa relativt ospecifika behandlingar. För denna grupp saknas idag behandlingsalternativ vilket leder till en oönskad högre dödlighet. Men också för de barn som överlever sin leukemi kan den ospecifika och toxiska behandlingen orsaka svåra och livslånga biverkningar. Därför är behovet av nya terapier, som ger mindre biverkningar och som framför allt kan hjälpa de barn som inte svarar på standardbehandlingarna, väldigt stora.
Hitta nya terapier - ett mål
ALL har länge studerats med hjälp av genetiska verktyg som har en betydande roll i klassificeringen av sjukdomen i olika riskgrupper, men analyserna har inte använts för utveckling av effektivare och mer precisa behandlingar med färre biverkningar. Barncancerfonden har därför finansierat en studie där forskarna tagit fram ett dataset där en panel av 49 ALL-cellinjer genomgått masspektrometri-baserad analys av proteomet, RNA-sekvensering, genfusionsanalys samt läkemedelsscreening för att se hur biologiska skillnader påverkar effekten av 528 olika läkemedel.
Rozbeh Jafari, senior forskningsspecialist på Karolinska Institutet har lett gruppen som tagit fram analysverktyget.
– Vi har utvidgat våra analysmetoder och inkluderat proteomik samt läkemedelsscreeningar för att lättare kunna identifiera alternativa terapier för vissa identifierade högriskgrupper, men vi kan också lära oss mer hur dessa mer specifika terapier funkar.
Biologiska skillnader påverkar resultatet
Det som är unikt med verktyget är att det för första gången erbjuder proteomik-data samt läkemedelskänslighet för ett stort antal cellinjer som etablerats från patienter med svårbehandlad ALL.
– Genom analysverktyget kan man på ett enkelt sätt se nivåer av över 12 000 proteiner, uttrycket av cirka 19 000 RNA fragment och läkemedelskänslighet för 528 olika läkemedel i dessa cellinjer, berättar Rozbeh Jafari.
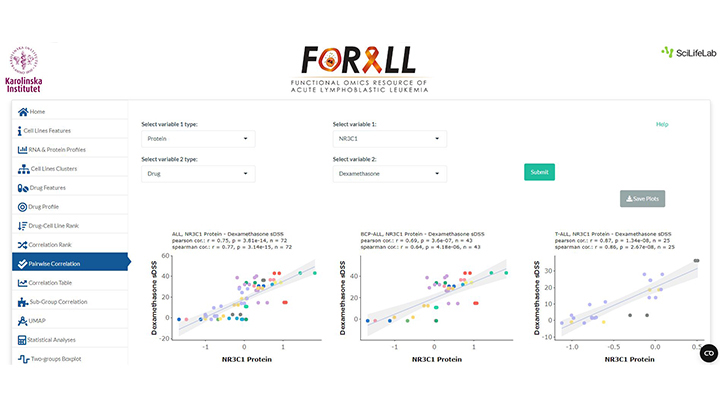
– Man kan se hur olika subtyper av ALL svarar på ett visst läkemedel eller om de är extra känsliga mot vissa klasser av läkemedel. I verktyget kan vi göra egna grupperingar och analyser samt studera relationen mellan läkemedelskänslighet och nivåerna av specifika proteiner för att se vad som kan styra resistens.
Och studien har gett ny kunskap vilket bland annat presenterats i en artikel i den högt ansedda vetenskapliga tidskriften Nature Communications under våren.
– Vi har med hjälp av proteomikanalys och läkemedelscreening av cellinje-modeller kunnat visa att proteinerna i cellerna är bättre markörer för att studera sjukdomens biologi än traditionella genetiska metoder samt för att identifiera läkemedelsmekanismer och de egenskaper som gör leukemicellerna känsliga för eller resistenta mot vissa läkemedel. Vi kunde även identifiera en oväntad känslighet hos celler från en högriskgrupp mot en typ av läkemedel som påverkar de molekylära signalerna som normalt aktiverar immunceller.
Offentlig resurs
Det senare väcker hopp om att kunna identifiera nya terapier som ger mindre biverkningar eller kan användas vid de subtyper av ALL som idag inte svarar så bra på dagens standardbehandling. Rozbeh Jafari hoppas nu att andra forskare ska använda analysverktyget för att initiera andra forskningsprojekt.
– Vi kombinerade våra omfattande dataset och byggde ett webbaserat verktyg för att andra forskare lättare ska kunna navigera i vårt data, analysera och hitta nya intressanta fynd men även för att kunna validera egna, tidigare fynd i våra dataset. Vi ser redan att verktyget har använts av forskare från hela världen.


